
- English
- Español
- Português
- русский
- Français
- 日本語
- Deutsch
- tiếng Việt
- Italiano
- Nederlands
- ภาษาไทย
- Polski
- 한국어
- Svenska
- magyar
- Malay
- বাংলা ভাষার
- Dansk
- Suomi
- हिन्दी
- Pilipino
- Türkçe
- Gaeilge
- العربية
- Indonesia
- Norsk
- تمل
- český
- ελληνικά
- український
- Javanese
- فارسی
- தமிழ்
- తెలుగు
- नेपाली
- Burmese
- български
- ລາວ
- Latine
- Қазақша
- Euskal
- Azərbaycan
- Slovenský jazyk
- Македонски
- Lietuvos
- Eesti Keel
- Română
- Slovenski
- मराठी
- Srpski језик
Kit de transporte de vírus da BABIO obtém autorização FDA 510(k)
Kit de transporte de vírus da BABIO obtém autorização FDA 510(k)
Jinan, China – outubro de 2025— BABIO Biotechnology, um renomado fabricante chinês de reagentes para diagnóstico médico, orgulhosamente anuncia que seuKit de transporte de vírus (não inativador)recebeuAutorização FDA 510(k) (K250205), validando oficialmente sua conformidade com os padrões regulatórios dos EUA.
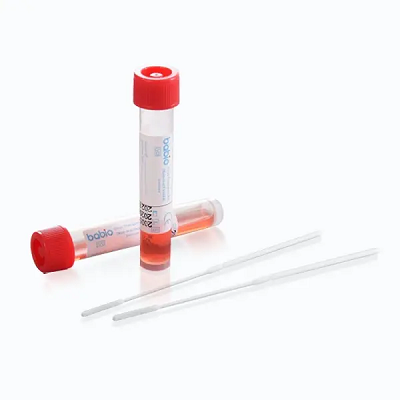
Este marco reforça a liderança global da BABIO em soluções de transporte de amostras clínicas. O kit foi projetado para coleta segura e estável de amostras virais, suportando aplicações downstream, comoRT-PCR, cultura viral, ediagnóstico molecular. Possui:
-
✅ Estabilidade da temperatura ambiente
-
✅ Solução melhorada de Hank com antibióticos
-
✅ Tubos cônicos livres de DNase/RNase
-
✅ Cotonetes flocados seguros com design de ponto de interrupção
Disponível em vários volumes de enchimento (1ml a 6ml) e tamanhos de embalagem (20 a 500 tubos), o kit é ideal para hospitais, laboratórios e instituições de saúde pública em todo o mundo.
Com umcapacidade de produção diária de 100.000 unidades, a BABIO garante fornecimento consistente e preços competitivos. Confiei noEstados Unidos, Alemanhae muito mais, a BABIO continua a oferecer inovação e confiabilidade em sistemas de transporte de vírus.Saiba mais em https://www.babiocorp.com.
#VirusTransportKit #FDA510k #BABIO #ClinicalDiagnostics #VTM #RT-PCR #GlobalHealthcare #MedicalDevices #SpecimenCollection


